L'eau est une espèce chimique omniprésente, à l'état liquide dans la gamme ordinaire de température
et de pression au quotidien. De nombreuses autres espèces chimiques peuvent se mélanger avec elle.
Chaque espèce chimique est caractérisée par sa solubilité dans l'eau à une température donnée,
grandeur qui indique la masse maximale qu'il est possible de dissoudre dans un iltre de mélange.
À partir d'eau et d'une espèce à dissoudre. Par exemple avec du sucre versé dans un café. En agitant le mélange avec la cuillère, le sucre est dissous dans la solution. On parle alors de dissolution. On peut également dissoudre un soluté à l'état liquide dans l'eau. C'est le cas par exemple en fabriquant un gel hydro-alcoolique : de l'alcool, à l'état liquide, est versé dans de l'eau et y est dissous.
Une autre méthode consiste à se munir d'une solution déjà existante et à y rajouter de l'eau. C'est l'opération
qu'on réalise chez soi lorsqu'on se prépare un verre de sirop, par exemple. On parle alors de dilution.
La notice qui figure sur les bouteilles de sirop indique la marche à suivre, c'est-à-dire le protocole
pour préparer un verre de boisson ; par exemple : "Dans un verre, verser une dose de sirop puis ajouter neuf
doses d'eau." Comme une dose de sirop permet d'obtenir un volume total de dix doses de boisson, la boisson
fabriquée sera dix fois moins concentrée en sucre que le sirop de départ.

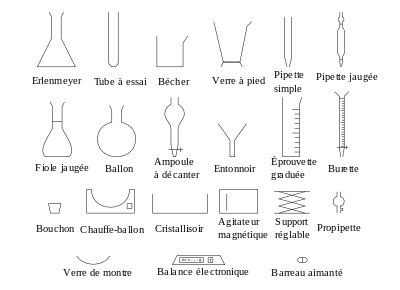
Au laboratoire, une solution aqueuse est toujours préparée dans une fiole jaugée pour connaître avec précision le volume de la solution obtenue. Les solides sont pesés avec une balance et les liquides sont prélevés avec une éprouvette graduée ou, plus précis encore, une pipette jaugée.